Статья на тему Эмбриональные стволовые клетки человека
Работа добавлена на сайт bukvasha.net: 2015-06-29Поможем написать учебную работу
Если у вас возникли сложности с курсовой, контрольной, дипломной, рефератом, отчетом по практике, научно-исследовательской и любой другой работой - мы готовы помочь.

Предоплата всего

Подписываем
Сергей Львович Киселев, проф., д.б.н., зав. лаб. молекулярной генетики рака Ин-та биологии гена РАН. Мария Андреевна Лагарькова, к.б.н., рук. группы биологии стволовых клеток в том же институте.
Пожалуй, самым молодым направлением современной медицины можно считать клеточные технологии, в которых клетки служат источником тех или иных необходимых факторов, например опухолевых антигенов при вакцинотерапии. Но использовать клетку можно не только как источник каких-либо субстанций, но и для регенеративной медицины. Здесь особый интерес вызывают технологии, основанные на стволовых клетках. Способность к неограниченному делению и к преобразованию в разные типы клеток (так называемая плюрипотентность) делает их идеальным материалом для трансплантационных методов терапии. Наиболее доступными считаются стволовые клетки взрослого организма. Однако реальный потенциал их дифференцировки еще слабо изучен.
Чрезвычайно привлекательны в этом отношении эмбриональные стволовые клетки (ЭСК) человека: из них можно получать любые типы клеток организма. Но многие свойства и клеточные механизмы, связанные с наличием у клетки так называемой «стволовости», ставят ее очень близко к трансформированной, раковой клетке. Именно поэтому так важно сегодня изучать характеристики самих эмбриональных клеток. За восемь лет, прошедших с момента получения первых линий ЭСК человека, удалось выяснить лишь небольшую часть механизмов, обеспечивающих в культуре самоподдержание недифференцированных клеток или их дифференцировку.
Еще недавно количество линий ЭСК человека, доступных для изучения, было невелико. В настоящее время их стало гораздо больше, но методологические трудности и высокая стоимость работы с ними еще ограничивают круг исследователей. Не меньшие ограничения на исследования в области эмбриональных клеток человека накладывает этическая сторона. Несмотря на дебаты об этичности или неэтичности работы с ЭСК человека, очевидно, что вопрос уже не в том, проводить ли исследования в области ЭСК человека, а в том, как будут проводиться исследования в этой области. За последние два года в большом числе стран уже были приняты законы, разрешающие исследования эмбриональных стволовых клеток человека.
Эмбриональные стволовые клетки получают из внутренней клеточной массы бластоцисты на самых ранних стадиях развития эмбриона, когда она еще не имплантировалась в стенку матки. Именно из клеток внутренней клеточной массы в дальнейшем развивается целый организм. Довольно часто, особенно в русскоязычной литературе, эмбриональными стволовыми клетками называют клетки постимплантационного эмбриона различных сроков развития беременности, которые по своим свойствам скорее схожи с взрослыми стволовыми клетками. Мы же будем говорить только об истинных эмбриональных стволовых клетках, происходящих из бластоцисты, - на той стадии, когда эмбрион состоит из 150-200 клеток трофоэктодермы и внутренней клеточной массы примерно в равном соотношении.
Стабильные линии
Стабильные клеточные линии ЭСК человека впервые получил американский исследователь Дж.Томсон в 1998 г. [1]. Этому достижению предшествовали работы М.Эванса и М.Кауфмана. В 1981 г. они впервые показали принципиальную возможность получения стабильных культур клеток млекопитающих, обладающих свойством плюрипотентности. Линии ЭСК мыши оставались в культуре in vitro в недифференцированном состоянии на протяжении более сотни удвоений, а потом in vivo могли участвовать в формировании специальных тканей животного. В 1995 г. Томсон с коллегами, модифицировав технологию выделения мышиных клеток, получил линию ЭСК приматов, а в 1998 г. - и линию клеток человека.
Для получения стабильных линий ЭСК человека берут невостребованные после искусственного оплодотворения бластоцисты человека. Обычно после такой процедуры количество бластоцист больше, чем необходимо реципиенту. Их можно заморозить, уничтожить либо с согласия доноров использовать для научных целей. Лучше всего выделять эмбриональные клетки человека на 4-6-й день после оплодотворения. Сначала с помощью фермента проназы растворяют прозрачную оболочку бластоцисты, а затем методом комплемент-зависимого лизиса удаляют трофобласты. Внутреннюю клеточную массу помещают в культуральную среду на подложку из инактивированных мышиных эмбриональных фибробластов, которые служат источником ростовых факторов. Пересаживая клетки, можно получить клеточную линию, способную к практически неограниченному делению. Сегодня в лабораториях мира выделено около 150 линий ЭСК. В нашей стране эмбриональные стволовые клетки получены в 2003 г. в Институте биологии гена РАН и в Институте цитологии РАН.
Рис. 1. Три колонии ЭСК человека.
В отличие от ЭСК мыши, человеческие клетки очень плохо растут в виде одиночных клеток,
а выживают только в колонии. Увел. 100. Здесь и далее фото авторов Эмбриональные стволовые клетки растут плотными колониями клеток на подложке из митотически инактивированных эмбриональных фибробластов мыши (рис.1). Успешность получения линий ЭСК человека довольно высока при использовании морфологически нормальных бластоцист с видимой внутренней клеточной массой, почти половина которых может дать кариотипически нормальные клетки. Эти результаты соответствуют уровню имплантации эмбрионов после пересадки реципиентам. Наращивать клеточную массу довольно сложно. Мышиные клетки прекрасно растут после ферментативной обработки до единичных клеток, но клетки человека, лишенные межклеточных контактов, обычно гибнут. Поэтому их разделяют до отдельных фрагментов по 50-500 клеток (либо ферментативной обработкой, либо механически, разрезая на кусочки микроинструментами).
Манипуляции с ооцитами in vitro позволяют получать линии ЭСК человека с заданным генотипом и, соответственно, иммунологически совместимые с потенциальным донором. Здесь возможно несколько подходов: перенос ядер соматических клеток, партеногенез или слияние клеток. Перенос ядер соматических клеток довольно часто не совсем корректно называют клонированием. В последние месяцы 2005 г. развернулась детективная история вокруг работ ученых из Сеульского национального университета под руководством В.Хванга. В 2004-2005 гг. в журнале «Science» они опубликовали две работы с описанием методики получения линии ЭСК человека из внутренней клеточной массы, полученной после пересадки ядра соматической клетки в ооцит. К сожалению, работы оказались грандиозной фальсификацией, причины которой до сих пор не выяснены. Не исключено, что все могло быть заранее организовано третьими лицами в коммерческих либо политических целях. Однако эти события не только не снизили интерес к проблеме, но и активизировали работы в этом направлении.
Основные характеристики
Как и все клеточные культуры, эмбриональные стволовые клетки нуждаются в четкой характеристике [2]. Самое простое - это внешнее описание, но оно дает весьма ограниченную информацию о свойствах клеток. В последнее время принято различать клетки по поверхностным антигенам, которые более полно описывают тот или иной тип. Эмбриональные стволовые клетки человека имеют поверхностные иммунологические маркеры, например: SSEA-3, SSEA-4 - антигенные детерминаты (эпитопы) гликолипидов и TRA-1-60, TRA-1-81 - разные эпитопы одного протеогликана клеточной поверхности.
Наличие набора определенных маркеров говорит о принадлежности клеток к ЭСК человека, но не об их способности к длительной пролиферации. Она определяется активностью фермента теломеразы и длиной теломерных повторов. У соматических клеток с ограниченным числом делений длина теломер мала, а теломеразная активность обычно очень невысока. Напротив, у опухолевых клеток активность фермента остается очень высокой, а длина теломерных повторов сохраняется. Этим же свойством обладают и эмбриональные стволовые клетки.
И иммунологические маркеры ЭСК, и высокая теломеразная активность присущи трансформированным клеткам, т.е. клеткам, в которых произошли генетические изменения. Значит, для точной характеристики линий ЭСК человека обязателен анализ кариотипа. Нормальный набор хромосом и отсутствие хромосомных аномалий - это признаки нормального кариотипа, который, однако, в процессе культивирования клеток может быть нарушен. Так, при длительном культивировании (примерно через два года) мы отметили существенное изменение в скорости роста клеток, а также в их способности к дифференцировке. Кариотипический анализ показал нарушения в хромосоме 18 и тенденцию к нестабильности кариотипа. Не исключено, что это и стало причиной аномального поведения клеток в культуре. Впоследствии мы не раз обнаруживали субклоны других линий ЭСК с различными хромосомными аберрациями. Совсем недавно появилась публикация, подтверждающая наши наблюдения. Следовательно, при длительном культивировании ЭСК человека необходим строгий контроль их кариотипа.
Молекулярно-генетические механизмы самоподдержания
Одно из замечательных свойств эмбриональных стволовых клеток - их способность сохранять плюрипотентность в культуре. На мышиных клетках это легко проверить экспериментально: из одной клетки, культивируемой in vitro, можно воссоздать целый организм. Именно так получают животных с генетическим «нокаутом». Суть технологии заключается в том, что генетически модифицированные in vitro эмбриональные клетки мыши вводят в бластоцисту, которую имплантируют псевдобеременной мышке. В результате рождаются так называемые химерные мыши, у которых часть клеток - от бластоцисты реципиента, а часть генетически модифицирована. Если такие клетки попадут в зародышевый путь, во втором поколении можно получить животное, все клетки которого будут потомками одной генетически модифицированной эмбриональной клетки.
Эта технология не только позволяет «выключать» определенные гены в строго детерминированных тканях, но «включать» дефектные, создавая модельные системы заболеваний. По понятным причинам такая процедура с клетками человека невозможна. Здесь для проверки плюрипотентности эмбриональные клетки человека вводят иммунодефицитным мышам. В результате у животных формируются доброкачественные опухоли - тератомы, в которых можно обнаружить несколько видов сформировавшихся тканей [3]. Однако для постоянного мониторинга состояния ЭСК и для обеспечения оптимальных условий культивирования такой метод представляется нерациональным. Здесь очень важно выяснить молекулярные механизмы, определяющие специфику эмбриональных стволовых клеток, а именно их способность оставаться в культуре в недифференцированном состоянии. Некоторые механизмы - общие для ЭСК мыши и человека, а некоторые - различны.
В самоподдержании ЭСК участвует транскрипционный фактор OCT4, который проявляется с восьмиклеточной стадии эмбриона мыши. Он необходим для формирования внутренней клеточной массы бластоцист (в клетках трофоэктодермы он отсутствует). Соответствующая активность гена oct4 поддерживает недифференцированное состояние эмбриональных клеток, а ее повышение или отсутствие вызывает их преобразование в клетки энтодермы и мезодермы или трофобласта соответственно [4]. В клетках соматических тканей экспрессия гена oct4, характерная для ЭСК человека, не обнаружена, хотя в последнее время появились сообщения о его низкой активности в стволовых клетках взрослого организма. Даже в начале дифференцировки ЭСК в эмбриоидные тельца активность гена оct4 снижается.
В поддержании плюрипотентности ЭСК мыши и человека участвует также гомеобоксный транскрипционный фактор NANOG. Если ген nanog заблокирован, эмбриональные клетки превращаются в примитивную энтодерму. В отсутствие ростового фактора LIF повышенная активность гена nanog обеспечивает плюрипотентное состояние ЭСК мыши. Подобно гену oct4, в клетках соматических тканей ген nanog не проявляется, за исключением фетального мозга, репродуктивных органов (семенников и яичников) и клеток эмбриональной карциномы. По мере спонтанной дифференцировки ЭСК человека в эмбриоидные тельца активность гена nanog снижается.
Кроме генетических механизмов, судьбу клетки определяют и так называемые эпигенетические механизмы (т.е. наследуемые клеткой изменения в функционировании генов, не связанные с изменением последовательности ДНК). Ярким примером их действия может служить инактивация одной из Х-хромосом в женских ХХ-клетках. Эпигенетические механизмы играют существенную роль в процессах раннего эмбрионального развития, контролируя работу генов. Эпигенетическая модификация регуляторных районов генов обеспечивает выключение их функций на последующих этапах развития. Это чрезвычайно важно, поскольку несвоевременная либо нескоординированная работа генов может приводить к гибели клеток или к их трансформации. Например, регуляторный район гена oct4 эпигенетически модифицирован практически во всех клетках взрослого организма. Такое изменение и составляет одну из основных проблем переноса ядер соматических клеток взрослого организма в ооцит. В нашей лаборатории показано, что и регуляторный район гена nanog в клетках взрослого организма эпигенетически модифицирован, что еще больше усложняет перенос ядер.
Современные методы анализа, такие как микрочипы, позволяют достаточно быстро определять активность нескольких тысяч генов, что создает более точную картину молекулярно-генетического состояния клетки. Это особенно важно для длительно культивируемых клеток, предназначенных для терапии.
Говоря о поддержании плюрипотентности эмбриональных стволовых клеток млекопитающих, нельзя не отметить роль внешних ростовых факторов, в том числе и фибробластов в качестве подложки-фидера (от англ. feed - кормление, питание). Первые клеточные линии ЭСК мыши и человека получали с использованием первичных мышиных эмбриональных фибробластов, обеспечивающих не только лучший рост клеток, но и их недифференцированное состояние. Позднее их заменили бессмертной клеточной линией. Однако считается, что эти клеточные линии нельзя применять в регенеративной медицине или генной терапии, поскольку от мышиных клеток возможен перенос патогенных микроорганизмов и вирусов. Кроме этого, клетки человека начинают представлять мышиные антигены, что может вызвать отторжение трансплантата. Сегодня для культивирования линий ЭСК человека иногда используются фибробласты крайней плоти человека. В литературе появились отдельные публикации о получении таких линий и в бесфидерных условиях.
Дифференцировка in vitro
In vitro спонтанная дифференцировка ЭСК происходит при длительном культивировании прикрепленных колоний и в суспензии по мере роста эмбриоидных телец, которые до некоторой степени служат моделью ранних событий эмбриогенеза. В случае мышиных ЭСК эмбриоидные тельца получаются аггрегированием отдельных клеток или групп клеток в сферические структуры. В отличие от мышиных клеток, не все линии человека легко образуют эмбриоидные тельца, и никогда из одиночных клеток. В эмбриоидных тельцах короткого культивирования наблюдаются группы клеток, несущие маркеры, специфические для всех трех зародышевых листков (рис.2), но дальше развитие останавливается. Сегодня четкого ответа о причинах торможения органогенеза нет; вероятнее всего, для этого нужна поляризация эмбриона, диктуемая извне.
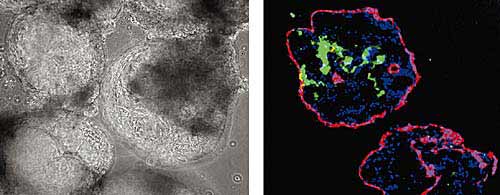
Рис. 2. Эмбриоидные тельца, сформированные ЭСК человека.
По мере созревания внутри плотных клеточных шариков появляются полости, и через некоторое время эмбриоидное тельце превращается в сферу. Справа показано иммуногистохимическое окрашивание срезов эмбриоидных телец антителами к клеткам эпителия (красный), мезодермальным клеткам (зеленый), синим окрашены ядра клеток. Увел. 50.
Эмбриональные стволовые клетки in vitro способны преобразоваться в различные клетки, имеющие специфические маркеры нейронов и глии, эндотелия, кератиноцитов, трофобластов, кардиомиоцитов, остеобластов, клеток крови, гепатоцитов, инсулин-продуцирующих клеток и некоторых других [2]. Однако функциональность большинства носителей маркеров еще мало доказана.
В 2001 г. впервые описали дифференцировку ЭСК человека в нейроны и астроциты [5]. Клетки нейроэктодермы, формирующиеся в эмбриоидных тельцах, механически извлекали, помещали в соответствующие условия культивирования (факторы, обеспечивающие пролиферацию клеток), где формировались нейросферы. Hейральные предшественники после пересадки в мозг новорожденных мышей могли образовывать три типа нейральных клеток и не давали тератом.
С тех пор сделано очень много. Найдены факторы, увеличивающие количество нейральных предшественников (ретиноевая кислота, блокатор cигнального пути BMP и др.); показана дифференцировка функциональных нейрональных клеток определенной специализации (например, дофаминергических нейронов). Недавно получены данные о возможности длительного (более 100 пассажей) культивирования нейроэктодермальных предшественников в бессывороточной среде в присутствии ростовых факторов.
Нейрональные предшественники получают через стадию эмбриоидных телец или напрямую из недифференцированных колоний линий ЭСК человека. Нейрональные предшественники можно культивировать в суспензии до 25 пассажей в виде нейросфер в присутствии эпидермального фактора роста и фактора роста фибробластов. При переводе нейросфер на культуральный пластик, покрытый компонентами внеклеточного матрикса, они прикрепляются и преобразуются в нейроны и астроциты. При добавлении в среду трииодтиронина и определенных ростовых факторов в нейросферах появляются предшественники олигодендроцитов. Вероятно, именно олигодендроциты и будут первыми клетками, полученными из ЭСК человека, которые пройдут апробацию при клинических испытаниях лечения травмы спинного мозга. Эти клетки, секретирующие основной белок миелина, необходимы для восстановления поврежденного участка нервной ткани спинного мозга. В США эти испытания планируют начать уже в 2006 г.
Спонтанную дифференцировку ЭСК в кератиноциты из эмбриоидных телец описали в 2003 г. Авторы отметили изменения активности трех маркеров, характерных для формирующихся кератиноцитов (p63, кератин 14, инволюкрин).
Эмбриональные клетки мыши легко дифференцируются в кардиомиоциты. Всего через несколько дней после удаления питательного слоя и фактора LIF, поддерживающего недифференцированное состояние клеток, на культуральных чашках образуются сокращающиеся колонии клеток. В определенных условиях они имеют электрофизиологию нормальных взрослых кардиомиоцитов и, более того, могут функционально интегрироваться в мышцу миокарда. В отличие от мышиных клеток, спонтанная дифференцировка клеток человека наблюдается у разных линий ЭСК - от сокращающихся участков в 70% эмбриоидных телец до полного отсутствия дифференцировки. Предшественники кардиомиоцитов, полученные из ЭСК человека, синтезируют транскрипционные факторы Nkx 2.5, GATA4, а затем и специфические маркеры кардиомиоцитов (тропонин 1 и тяжелую цепь -миозина). Мы наблюдали спонтанную дифференцировку ЭСК в кардиомиоциты в двух линиях из трех, причем сокращающиеся участки отмечались в очень небольшом проценте эмбриоидных телец.
Клетки гемопоэтического ряда впервые получили при совместном культивировании ЭСК человека с линиями стромальных фибробластов, а также используя факторы роста гематопоэтических клеток. В эмбриоидных тельцах обнаружена также популяция клеток, обладающих свойствами предшественников гематопоэтических клеток и эндотелиальных (гемангиобласт).
В нашей лаборатории ведутся работы по прямой (т.е. минуя стадию эмбриоидных телец) дифференцировке ЭСК человека в клетки эндотелия и разрабатываются методы их селекции. Используя коллагены в качестве матрикса, специальную среду и ростовые факторы, мы получили клеточные популяции, в которых эндотелиальные клетки составляют около 50%. На коллагеновом матриксе они образуют капилляроподобные структуры, несущие специфические маркеры сосудистого эндотелия (рис.3). Мы успешно применяли метод иммуномагнитной селекции СD31-положительных эндотелиальных предшественников на ранних (4-5-й день) этапах дифференцировки, поскольку на поздних этапах межклеточные контакты в капилляроподобных структурах с трудом поддаются энзиматическому расщеплению и клетки теряют жизнеспособность. В результате селекции нам удавалось выделить гомогенную популяцию эндотелиальных клеток, in vitro формирующих капилляроподобные структуры.
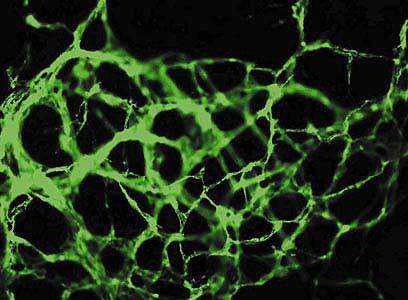
Рис. 3. Эндоваскулярная сеть, образованная in vitro чистой выделенной популяцией клеток эндотелия,
полученных методом иммуномагнитной сепарации из ЭСК человека (окрашена на маркер CD31). Увел. 200.
Труднее всего оказалось с производными энтодермы. Несмотря на опубликованные сообщения о дифференцировке ЭСК человека в инсулин-секретирующие клетки и гепатоциты, их функциональность не показана. Более того, по белковым и генетическим маркерам они не полностью совпадают с зрелыми инсулин-секретирующими клетками или гепатоцитами. Пока неизвестны факторы, определяющие преобразование в энтодерму, и маркеры ранней энтодермальной дифференцировки.
Итак, сегодня ясно, что для наработки массы клеток разных типов уже имеется разработанная модель дифференцировки, которая должна соответствовать определенным требованиям:
- эмбриональные стволовые клетки нужно культивировать в стандартизованных условиях с отработкой генетических манипуляций и соблюдением технологии клонального роста;
- индуцированную дифференцировку необходимо вести преимущественно к желаемому клеточному фенотипу и иметь возможность селекции нужных популяций клеток;
- все этапы дифференцировки должны быть воспроизводимы и контролируемы, а действие факторов, ее индуцирующих, хорошо известно;
- желательно также избегать многокомпонентных нестандартизованных факторов, таких как сыворотка, кондиционированная среда, клеточные экстракты и т.д.
Таковы научно-технологические аспекты разработки клеточных технологий на основе ЭСК человека. Одновременно с этим существует целый ряд этических проблем, связанных с исследованием и применением человеческих ЭСК.
Вокруг линий ЭСК человека продолжаются бесконечные дебаты, касающиеся моральной стороны проблемы, а именно возможного использования невостребованных бластоцист для выделения ЭСК. Ответа на этот вопрос до сих пор нет. Здесь хочется привести высказывание известного ученого в области раннего эмбрионального развития профессора В.Рейка: «Пока с помощью этой технологии кого-нибудь не спасут, разговоры об этичности и запреты на исследования не прекратятся».
Стремительное развитие исследований в области стволовых клеток человека стимулировало штат Калифорния принять Предложение 71 о выделении 3 млрд долл. на 10 лет для получения новых клеточных линий ЭСК. В мае 2005 г. Национальная академия наук США призвала к добровольному принятию этических правил в области исследования ЭСК человека. Эти правила касаются информированного согласия доноров, запрещения оплаты донорского материала, работы банков ЭСК, создания наблюдательных комитетов. Все 23 предложенных правила приняты к исполнению академическими и научными организациями штата Калифорния, вовлеченными в работу с ЭСК человека. Чуть позже FDA (Food and Drug Administration) издала инструкцию по скринингу и тестированию доноров человеческих клеток, тканей и продуктов, основанных на клетках. В некоторых странах Европейского сообщества в течение 2004-2005 гг. принят ряд законов, разрешающих исследования в области ЭСК человека.
Уже активно обсуждаются правила проведения первой фазы клинических испытаний на основе клеток, полученных из ЭСК человека. При этом преследуется основная цель - не навредить будущему реципиенту, поскольку эти трансплантаты существенно отличаются от традиционных. Во-первых, значительный период проходит между получением биологического материала и его применением. За это время могут обнаружиться новые заболевания доноров или те, которые не смогли определить при получении биологического материала. Кроме инфекционных, с течением времени у доноров клеточного материала могут проявиться генетические заболевания, в том числе такие, как наследственная предрасположенность к раку. Более того, применение иммуносупрессоров при трансплантации реципиентам аллогенного материала повышает риск онкологических и инфекционных заболеваний. И, наконец, если пересадка материала, полученного на основе ЭСК человека, окажется эффективной, то материал единичных линий будет применяться для большого количества пациентов. Поэтому одной из основных этических проблем, ожидающих клеточную терапию на основе ЭСК человека, будет проблема повторного контакта и обследования доноров биологического материала. Таким образом, развитие клеточных технологий на основе аллогенного материала, в том числе и ЭСК, приводит к новым вопросам этического характера, разрешить которые необходимо до начала клинических испытаний.
Итак, сегодня рано говорить о применении клеточных имплантатов, полученных на основе ЭСК человека. Остается слишком много нерешенных задач, главные из которых заключаются в безопасности использования таких имплантатов. Их реальную эффективность и безопасность можно будет оценить лишь после проведения длительных и тщательных клинических испытаний. Тем не менее, по оценке многих зарубежных консалтинговых компаний, технологии на основе ЭСК будут применяться в клинике уже на рубеже 2012-2015 гг.
Список литературы
1. Thomson J.A., Itskovitz-Eldor J., Shapiro S.S. et al. // Science. 1998. V.282. №5391. P.1145-1147.
2. Pera M.F., Trounson A.O. // Development. 2004. V.131. №22. P.515-525.
3. Reubinoff B.E., Pera M.F., Fong C.Y. et al. // Nat. Biotechnol. 2000. V.18. №4. P.399-400.
4. Niwa H., Miyazaki J., Smith A.G. // Nat. Genet. 2000. V.24. №4. P.328-330.
5. Reubinoff B.E., Itsykson P., Turetsky T. et al. // Nat. Biotechnol. 2001. V.19. №12. P.1134-1140.